Novo Nordisk Terima Peringatan FDA Pasca Inspeksi di AS
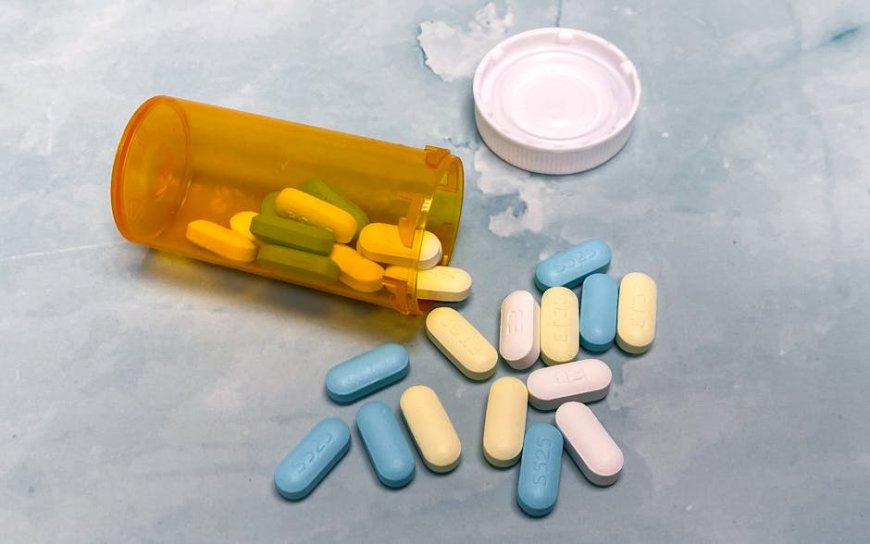
VOXBLICK.COM - Raksasa farmasi global, Novo Nordisk, baru-baru ini menerima surat peringatan (Warning Letter) dari Badan Pengawas Obat dan Makanan Amerika Serikat (FDA AS) menyusul inspeksi di salah satu fasilitas manufakturnya di Amerika Serikat pada awal tahun 2025. Pemberitahuan regulasi ini menandai momen penting bagi perusahaan Denmark tersebut dan menimbulkan pertanyaan serius tentang kepatuhan kualitas dalam industri farmasi yang sangat diatur.
Surat peringatan FDA adalah salah satu tindakan penegakan hukum paling serius yang dapat dikeluarkan oleh badan tersebut, mengindikasikan bahwa suatu perusahaan telah melanggar persyaratan regulasi signifikan, seringkali terkait dengan praktik
manufaktur yang baik (Good Manufacturing Practices/GMP). Meskipun rincian spesifik mengenai temuan inspeksi belum sepenuhnya dipublikasikan, peringatan semacam itu umumnya menyoroti defisiensi dalam sistem kualitas, kontrol proses, atau integritas data yang dapat memengaruhi keamanan, kemanjuran, dan kualitas produk obat.

Peristiwa ini menjadi perhatian khusus mengingat posisi Novo Nordisk sebagai pemain kunci dalam pasar farmasi global, terutama dengan popularitas obat-obatan revolusionernya seperti Ozempic dan Wegovy yang digunakan untuk diabetes dan penurunan
berat badan. Kepatuhan terhadap standar manufaktur tertinggi sangat krusial untuk menjaga kepercayaan publik dan memastikan pasokan obat-obatan penting yang stabil dan aman.
Latar Belakang Inspeksi dan Temuan Umum FDA
Inspeksi FDA adalah bagian rutin dari pengawasan regulasi untuk memastikan perusahaan farmasi mematuhi standar yang ketat dalam produksi obat.
Inspeksi ini dapat bersifat rutin atau dipicu oleh keluhan, masalah kualitas yang teridentifikasi, atau sebagai bagian dari proses persetujuan obat baru. Ketika inspektur FDA menemukan penyimpangan dari GMP, mereka akan mencatatnya dalam formulir 483. Jika penyimpangan tersebut dianggap serius dan tidak ditangani dengan memadai oleh perusahaan, FDA dapat meningkatkan tindakan menjadi surat peringatan.
Surat peringatan biasanya merinci pelanggaran spesifik yang diamati, memberikan kerangka waktu bagi perusahaan untuk merespons dengan rencana tindakan korektif (Corrective and Preventive Actions/CAPA) yang komprehensif.
Kegagalan untuk menanggapi secara memadai dapat mengakibatkan konsekuensi lebih lanjut, termasuk larangan impor, penyitaan produk, atau penolakan persetujuan aplikasi obat baru dari fasilitas yang bermasalah.
Meskipun rincian temuan spesifik di fasilitas Novo Nordisk belum diungkap secara luas, pengalaman menunjukkan bahwa surat peringatan farmasi sering kali berkaitan dengan:
- Defisiensi Sistem Kualitas: Kurangnya prosedur tertulis yang memadai atau kegagalan untuk mengikuti prosedur yang ada.
- Kontrol Proses yang Tidak Memadai: Masalah dalam pemantauan dan pengendalian parameter kritis selama proses manufaktur.
- Pengujian Produk yang Tidak Sesuai: Kegagalan untuk melakukan pengujian kualitas yang tepat atau adanya hasil pengujian yang tidak valid.
- Integritas Data: Masalah dengan pencatatan data yang akurat, lengkap, dan konsisten, yang sangat penting untuk melacak dan memverifikasi kualitas produk.
- Kondisi Fasilitas: Lingkungan produksi yang tidak memenuhi standar kebersihan atau desain yang sesuai untuk mencegah kontaminasi.
Implikasi Regulasi dan Bisnis bagi Novo Nordisk
Penerimaan surat peringatan FDA membawa serangkaian implikasi signifikan bagi Novo Nordisk, baik dari sisi regulasi maupun bisnis. Respons perusahaan terhadap peringatan ini akan diawasi ketat oleh regulator, investor, dan publik.
Dampak Regulasi:
- Peningkatan Pengawasan: Fasilitas yang bermasalah kemungkinan akan menghadapi inspeksi FDA yang lebih sering dan mendalam di masa mendatang.
- Penundaan Persetujuan: Aplikasi obat baru atau perubahan manufaktur yang melibatkan fasilitas yang terkena dampak dapat tertunda hingga semua masalah teratasi.
- Potensi Pembatasan Operasi: Dalam skenario terburuk, FDA dapat mengeluarkan larangan impor, menahan pengiriman produk, atau bahkan memerintahkan penghentian sementara operasi di fasilitas tersebut jika masalah kualitas tidak ditangani secara efektif.
Dampak Bisnis:
- Biaya Perbaikan: Perusahaan harus menginvestasikan sumber daya yang signifikan untuk mengatasi defisiensi yang ditemukan, termasuk perombakan sistem, pelatihan personel, dan peningkatan fasilitas.
- Risiko Reputasi: Surat peringatan dapat merusak reputasi perusahaan di mata pasien, penyedia layanan kesehatan, dan investor, yang berpotensi memengaruhi penjualan dan nilai saham.
- Gangguan Pasokan: Jika produksi terganggu, hal ini dapat menyebabkan kekurangan pasokan obat-obatan penting, yang memiliki konsekuensi serius bagi pasien dan pangsa pasar perusahaan.
- Tekanan Investor: Investor akan mencari kejelasan mengenai dampak finansial dan operasional dari peringatan tersebut, yang dapat memengaruhi sentimen pasar terhadap saham Novo Nordisk.
Novo Nordisk diharapkan akan merilis pernyataan resmi dan rencana tindakan korektif dalam waktu dekat untuk mengatasi kekhawatiran FDA.
Keberhasilan dalam menanggapi peringatan ini akan sangat bergantung pada seberapa cepat dan efektif perusahaan dapat mengimplementasikan perubahan yang diperlukan untuk memenuhi standar regulasi.
Dampak Lebih Luas pada Industri Farmasi Global
Insiden seperti surat peringatan FDA kepada Novo Nordisk memiliki riak yang meluas ke seluruh industri farmasi global.
Ini berfungsi sebagai pengingat tajam akan pentingnya kepatuhan regulasi yang tak tergoyahkan dan penekanan berkelanjutan pada kualitas produk.
Beberapa dampak yang lebih luas meliputi:
- Peningkatan Fokus pada Kualitas Manufaktur: Perusahaan farmasi lain mungkin akan meninjau ulang sistem kualitas internal mereka dan melakukan audit mandiri untuk memastikan mereka tidak menghadapi masalah serupa.
- Penekanan pada Integritas Data: Dengan semakin canggihnya teknologi, integritas data menjadi area fokus utama bagi regulator. Insiden ini dapat mendorong perusahaan untuk berinvestasi lebih banyak dalam sistem yang memastikan data yang akurat dan tidak dapat diubah.
- Peran Kunci Rantai Pasokan Global: Dalam ekonomi global, banyak obat diproduksi di berbagai negara. Surat peringatan ini menyoroti kerentanan dalam rantai pasokan global dan kebutuhan akan pengawasan kualitas yang konsisten di seluruh lokasi produksi.
- Perlindungan Pasien: Pada intinya, tindakan FDA bertujuan untuk melindungi kesehatan masyarakat. Setiap peringatan menegaskan kembali komitmen regulator untuk memastikan bahwa obat-obatan yang tersedia di pasar aman dan efektif.
Kasus Novo Nordisk ini menggarisbawahi bahwa bahkan perusahaan farmasi terbesar dan paling sukses pun tidak kebal terhadap pengawasan regulasi yang ketat.
Kepatuhan terhadap standar kualitas bukan hanya kewajiban hukum, tetapi juga pilar fundamental kepercayaan publik dan keberlanjutan bisnis dalam sektor farmasi.
Masa depan akan menunjukkan bagaimana Novo Nordisk menavigasi tantangan regulasi ini.
Respons yang cepat, transparan, dan efektif akan menjadi kunci untuk memulihkan kepercayaan, mengatasi defisiensi, dan terus memasok obat-obatan penting kepada pasien di seluruh dunia. Industri farmasi secara keseluruhan akan terus memantau situasi ini sebagai studi kasus tentang pentingnya mempertahankan standar kualitas tertinggi dalam setiap aspek operasi.
Apa Reaksi Anda?
 Suka
0
Suka
0
 Tidak Suka
0
Tidak Suka
0
 Cinta
0
Cinta
0
 Lucu
0
Lucu
0
 Marah
0
Marah
0
 Sedih
0
Sedih
0
 Wow
0
Wow
0



















































![[VIDEO] Rekor Dunia di Balik Suntikan Polio Massal Pertama Tahun 1955](https://img.youtube.com/vi/8eH0e--DOmU/hqdefault.jpg)
